مقاله ای از حمید رقمی/ نیترات و مشتقاتی از آن در آب و مواد غذائی (از کم خطرتا بسیار پرخطر)
بسپار/ایران پلیمر ابتدا یک توضیح الزامی :
نظر به اینکه اطلاعات وآمار قابل استنادی در رابطه با وجود نیترات در آب و مواد غذائی در ایران وجود ندارد ( یا وجود دارد و نگارنده این وبلاگ از آن بی اطلاع است )، در این پست به اطلاعات و آمارهای مربوط به این موضوع از کشور آلمان-که هم دقیق و علمی است و هم به روز- اجباراً بسنده می شود .
« نیترات؛ نیتریت؛ نیتروزوآمین» واژه هائی هستند که این روز ها کم و بیش از طرف افراد با سطح دانش متفاوت، مورد توجه و بعضاً پرسش قرار می گیرند. این موضوع بخصوص برای آنانی که توانائی مالی شان ” اجازه و امکان خوردن” برایشان – حتی در شرایط فعلی که قیمت ها سیر نجومی طی می کنند – میّسر است، بیشتر مورد توجه است. این گروه از افراد بطور معمول نسبت به ” آنچه که می خورند” حساسیت های بیشتری هم به خرج می دهند.
درخصوص (سه گروه) ترکیبات ذکرشده لازم است توجه داده شود که میزان، منبع، چگونگی آماده سازی و… همه فاکتور هائی هستند که نقش تعیین کننده در” بی خطر، کم خطرو یا پر خطر” بودن آن ها دارد. از این میان نیترا ت( به خودی خود) از بی خطر تا کم خطر ارزیابی می شود. حال و نظر به اینکه همین ماده برای سلامتی نسبتاً ” بی خطر “، با تبدیل به نیتریت “خطر آفرین” گردیده و مهم تر از آن اینکه با تبدیلِ نیتریت ایجاد شده در بدن به نیتروزوآمین، “بسیار پر خطر” می شود. نیتروزو آمین ها بطور قطع آثار بسیار مخرب تری نسبت به نیتریت و نیترات دارند.
نیترات
نیترات ها املاح نیتریک اسید ( HNO3) هستند که معمولاً بصورت مواد معدنی در زمین وجود دارند و به صورت کود شیمیائی ( غیر آلی و آلی) و ارگانیک به زمین های کشاورزی افزوده می شوند.
همچنین از املاح سدیم وپتاسیم نیترات ( و بعضاً نیتریت) به صورت ” افزودنی های مجاز” در برخی از مواد غذائی مانند پنیر، گوشت و مواد گوشتی فراوری شده مانند سوسیس و کالباس و … به عنوان مواد ” نگهدارنده * استفاده می شود.
این ” افزودنی های مجاز” عمدتاً جهت افزایش زمان نگهداری محصولات غذائی از طریق متوقف کردن فعالیت باکتری ها و بخصوص یک نوع باکتری مخرب با نام clostridium botulinum ، مورد استفاده قرار می گیرند.
* مواد نگهدارنده با شماره های * E-250 ؛ E-251 و E-252 (دراتحادیه اروپا)
* منبع : BfR Bundesinstitut für Risikobewertung ( انستیتو فدرال (آلمان) برای ارزیابی ریسک )
در حاشیه :
درآنچه که به نیترات ها مربوط می شود، لازم است اشاره شود که استرهای نیتریک اسید مانند گلیسرین نیترات، سلوز نیترات و… نیز درکاتگوری نیترات ها قراردارند که بعضاً (به غلط) اصطلاح ” نیترو” در مورد آن ها بکار برده می شود.
تفاوت نیترات با ( ترکیبات ) نیترو
استرهای نیتریک اسید بعضاً با واژه ” نیترو …” نیز بکار برده می شوند که نا صحیح است. از جمله این استرها (بخصوص) استر نیتریک اسید با گلیسرین ( یک الکل) است که در بسیاری از موارد با نام ناصحیح ” نیترو گلیسرین ” و همچنین استر این اسید با سلولز است که آن هم با نام (ناصحیح )” نیترو سلولز “، زبانزد خاص و عام است .
توضیح: زمانی می توان از ” نیترو” صحبت کرد یا نوشت که اتم نیتروژن بطور مستقیم به کربن وصل است مانند نیترو متان ، نیترو تولوئین و… (C-N ) ؛ درحالیکه در سلولز نیترات و مشابه، اتم نیتروژن به اکسیژن متصل است ( Cel…O-N) و نه به کربن ! ( بنابراین سلولز نیترات صحیح است و نه ” نیتروسلولز”)
ادامه مطلب
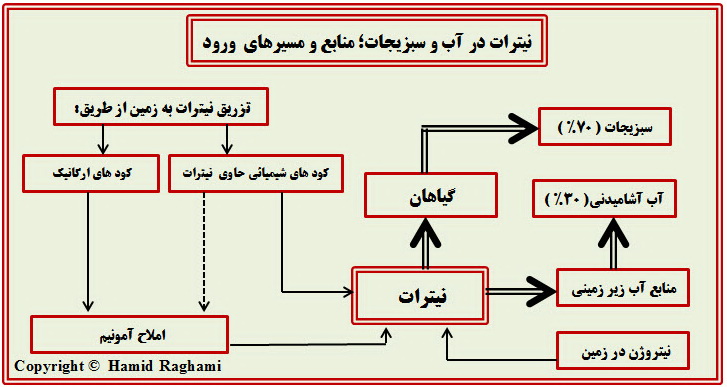
املاح نیتریک اسید یا نیترات ها معمولاً با غلظت های مختلف در زمین وجود داشته و در چرخه رشد و نمو گیاهای نقش تعیین کننده ای دارند. گیاهان از اتم های نیتروژن در نیترات ها، برای ساخت ترکیبات حاوی نیتروژن از جمله پروتئین های مورد نیاز و مصرف گیاهخواران درطبیعت ( و افراد گیاه خوار) استفاده می کنند. از پوسیدن نیترات در طبیعت در یک پروسه نسبتاً پیچیده، آمونیاک و املاح آمونیم ایجاد می شوند. این املاح از طریق پروسه ” نیتریفیکاسیون” به کمک باکتری های درون زمین مجدداً، به نیترات تبدیل می شوند. در طول پروسه نیتریفیکاسیون ( به عنوان واکنش های جانبی)، املاح نیتریت نیز ایجاد می شوند. از مهمترین املاح حاوی نیتروژن، می توان به آمونیم نیترات و پتاسیم نیترات اشاره کرد که از اولی بیشتر به عنوان کود غیر آلیِ حاوی نیترات و ازدومی بیشتر(درگذشته) برای ساخت باروت سیاه استفاده شده است.
( باروت سیاه متشکل از درصدهای مختلف از پتایسیم نیترات، پودر ذغالِ چوب و گوگرد است.)
استفاده نا متوازن و وسیع از املاح نیترات در محصولات زراعی، هم منابع آبی را آلوده می کند و هم قادر است از طریق مصرف سبزیجات و صیفی جاتِ حاوی نیترات، به خطرات زیادی برای سلامتی انسان منتهی گردد.
( در این خصوص بعداً توضیحاتی داده می شود)
نیتریفیکاسیون (Nitrification )
نیتریفیکاسیون (Nitrification) بخشی از چرخه نیتروژن در اکوسیستم است و عبارت است از تبدیل باکتریاییِ اکسیداتیوِ آمونیاک و املاح آمونیم حاصل از تجزیه بیو ماس (biomass ) به نیترات. اکسیژن مورد نیاز این فعل و انفعال از محیط جذب می شود و فرایند آن بصورت دو مرحله ای رخ می دهد. در مرحله اول آمونیاک به نیتریت و در مرحله دوم (سپس) نیتریت به نیترات، اکسید می شود. باکتری های موثر در این فرایند از انرژی آزاد شده در طول واکنش ها تغذیه می کنند. باکتری های دارای نقش در مرحله اول « نیتروزوموناس» و نوع دارای نقش در مرحله دوم « نیترو باکتر» نام دارند. املاح نیترات بدست آمده از این تغییر و تبدیل، به عنوان ترکیبات حاوی نیتروژن به مصرف تغذیه و رشد گیاهان می رسند.

نیترات درآب
موضوع ” نیترات در آب” (درکشور آلمان) نه تنها دغدغه ای جدی برای مصرف کنندگان است ، بلکه برای ارگان ها و مسئولان تأمین آب برای شهروندان نیز موضوعی بسیار با اهمیت تلقی می شود. در حال حاضر معضل نیترات در آب درگروه های مختلف جامعه آلمان از جمله مصرف کنندگان، ارگان های مسئول حکومتی، سازمان های مدافع حقوق مصرف کنندگان ، دانشمندان و سازمان ها غیر دولتی (NGO) به یک موضوع بسیار حیاتی و داغ تبدیل شده است. این حساسیت ها نسبت به موضوع ” نیترات درآب” بخاطر آثار وخیم و اثبات شده آن بر سلامتی انسان است. به اعتقاد صاحب نظران، علت (اصلی) وجود نیترات ( بالا) در آب، مصرف بی رویه انواع کود اعم از حیوانی و شیمیائی درکشاورزی می باشد.
ارقام مربوط به سال 2015 ( در کشور آلمان) حاکی از آن است که در استان « نیدر زاکسن» وجود 47% اجسام خارجی در منابع آب های زیر زمینی به نوعی به نیترات مربوط می شود. همچنین براساس اطلاعات آماری منتشر شده در سال های 2012 تا 2016 در اتحادیه اوپا، 28 درصد ایستگاه های اندازی گیری نیترات در آب، بالاتر از میزان مصوب شده یعنی 50 میلی گرم بر لیتر را به ثبت رساندند.
نیترات چگونه وارد منابع آب های زیر زمینی می شود؟
در کشور آلمان حدود 75% آب شرب از منابع زیر زمینی تأمین می گردد. از این منابع آب های زیر زمینی درکشاورزی نیز استفاده می شود. به اعتقاد ارگان های مسئو لِ حفاظت از آب در این کشور، میزان بالای نیترات در آب، رابطه مستقیم با نوع و میزان بهره برداری از زمین های کشاورزی دارد. استفاده از انواع کود ها و دیفوزیون املاح محلول در آّن ها به منابع آب، عامل اصلی ورود نیترات به این منابع است. در این میان کود های شیمیائی بیشتر از کودهای حیوانی، عامل وجود ارقام بالائی از نیترات در آب می باشند. یک مورد دیگر باید اضافه شود که آن این است که سیلوهای غیر استاندارد نگهدا ری انواع کود، از جمله کود های شیمیائی در بارندگی ها عامل انتقال نیترات به آب های سطحی و در دراز مدت به منابع آب زیر زمینی برشمرده می شوند. زمانی که میزان نیترات( به صورت انواع کودهای حیوانی و شیمیائی) که به زمین داده می شود، بیش از میزانی باشد که گیاهان برای رشد نیاز دارند، با باران و آب ناشی از ذوب شدن برف شسته شده، به لایه های پائین زمین وارد و نهایتاً در منابع آب های زیر زمینی جمع می شوند. بخش قابل توجه دیگری از نیترات حل شده در آب باران و برف های ذوب شده نیز از طریق آب راه ها به رودخانه ها و دریا ها وارد می شود.
چرا وجود نیترات در آب مشکل آفرین و خطرناک است؟
همانگونه که در بخش های دیگر این مقاله توضیح داده شد و می شود، نیترات به خودی خود (مستقیماً) زیانبار نیست. با این حال ولی در اثر ایجاد تغییرات ساختاری آن در ارگانیسم، به موادی خطر آفرین تبدیل می شوند. این تغییرات ساختاری بخصوص به کمک باکتری های درون روده – که هم متنوع هستند و هم به لحاظ تعداد به میلیون ها و بیشترنیز می رسند- رخ می دهند. از جمله این تغییرات ساختاری، می توان به تبدیل نیترات به نیتریت و سپس به نیتروزوآمین ها اشاره کرد. ازاین میان نیتریت بیشتر برای نوزادان و نیتروزو آمین ها بسیار خطرناک برای همه گروه های سنی می باشند.
مرزهای حد اکثری برای وجود نیترات ( و نیتریت) در آب
در راهنمای مصوبه شماره 118 (EG ) با عنوان EU-Grundwasserrichtlinie 2006/118/EG (GWRL) برای آب های زیر زمینی، میزان حداکثری نیترات 50 میلی گرم بر لیتر، تعیین گردیده است. در همین مصوبه آمده است که در صورت رسیدن میزان نیترات در آب به سه چهام از رقم ذکر شده، یعنی 37.5 میلی گرم برلیتر، اقدامات احتیاطی ضروری تشخیص داده شده اند.
برخلاف تعیین مرز حداکثری برای (سایر) مواد خطر آفرین که بر اساس وزن انسان اعلام می گردد ، میزان نیترات برای انسان در سنین مختلف متفاوت است، به طوری که در نوزادانِ کمتر از 3 ماه تا 6 ماه این رقم حد اکثری 10 میلی گرم بر لیتر تعیین گردیده و برای سایر گروه های سنی 50 میلی گرم بر لیتراست.
علت این موضوع در بخش نیتریت (در همین مقاله) تشریح گردیده است.

نیترات در مواد غذائی
محصولات غذائی گیاهی، بخصوص سبزیجات منابع مهمی برای انتقال به/ و جذب نیترات در بدن هستند. میزان نیترات موجود در انواع سبزیجات، بسیار متفاوت است. از سبزیجات حاوی نیترات بالا می توان به سبزیجاتی مانند اسفناج ، کاهو، چغندر، تربچه، کلم قمری( کلم سنگی) اشاره کرد.

از جمله عوامل این تفاوت ها، نوع و میزان ( تراکم) کود دهی است، با ذکر این نکته که سبزیجات ” ارگانیک” – اگر واقعاً ارگانیک باشند و نه آنگونه که بصورت عوام فریبانه متداول شده است – معمولاً حاوی نیترات کمتری هستند. همچنین میزان تابش نورخورشید به کاهش ذخیره نیترات در سبزیجات کمک می کند و به همین دلیل سبزیجات ” مزرعه ای”بخصوص در تابستان، حاوی نیترات کم تری می باشند. نیتراتِ محصولات مناطق جنوبی تر(اروپا) مانند سواحل مدیترانه ( تابش بیشتر نورخورشید) نیز به نسبت حاوی نیترات کمتری هستند. ضمناً اشاره شود که سبزیجات گلخانه ای معمولاً در صد های بیشتری نیترات در مقایسه با سبزیجات مزرعه ای دارند.

در اینجا لازم به تأکید است که نگهداری نا مناسب، گرم کردن دو باره ( وسه باره) سبزیجات پخته شده می تواند به افزایش میزان نیتریت از طریق واکنش های باکتری یائی بیانجامد. بخصوص در مورد اسفناج توصیه BfR بر آن است که مصرف تازه آن ترجیح داده شده و از گرم کردن مجدد آن پرهیزگردد. البته در برخی از خانواده ها در کشورعزیز خودمان متاسفانه و (نسبتاً )”معمول” است که نه تنها سبزیجات پخته شده، بلکه سبزیجات ” سرخ یا تفت داده شده”- آنهم بعضاً با روغن های جامد-که این نیز”داستانی” ست برای خود- مانند «قرمه سبزی»، کم و بیش بادمجان و… ماه ها در فریزر ( یا قسمت فوقانی یخچال !) ذخیره که نه، انبار می شوند ! !
دُز کُشنده ( letale Dosis) نیترات
دُز کُشنده ( letale Dosis) برای نیترات در انسان حدود 15 g است. نیتراتِ بخودی خود بی خطر، می تواند در ارگانیسم با ید (I )”رقابت”کرده و با جذب در تیروئید، عمل کِرد غده تیروئید را از مسیر اصلی خارج ویا دچار اختلال نماید.
در هرصورت وجود نیترات در بدن بنا بر مکتوبات سازمان ایمنی غذایی اروپا (European Food Safety Authority efsa ) و اداره فدرال( آلمان) برای ارزیابی خطر Budesamat für Risikobewertung , BfR (حداقل) به عنوان عاملی به نفع سلامتی تشخیص داده نشده است.
نیتریت
نیتریت ها املاح ” نیترو اسید ” (نیتروس اسید) (nitrous acid ) هستند که از واکنش اِحیاء نیترات (نیز) بدست می آیند.
حال و نظر به اینکه گیاهان نیتروژن مورد نیاز خود را از نیترات تأمین می کنند. می تواند نیتریت نیز در گیاهان به عنوان یک محصول جانبی از نیترات،(به مقدارکم)به کمک باکتری ها و آنزیم ها ایجاد گردد. این (مقدار کم) ولی با نگهداری و انبار کردن غیر اصولی، حمل و نقل غیر مناسب و غیر بهداشتی، از طریق ادامه واکنش های اِحیاء یا کاهشیِ باکتریائی، افزایش می یابد.
منبع: اداره فدرال (آلمان) برای ارزیابی ریسک (BfR, 2013)
نیتریت همچنین از طریق مواد افزودنی مجاز(پتاسیم و سدیم نیترات و نیتریت) که ذکر آن رفت نیز بعضاً به مواد غذائی مانند برخی از پنیر ها و مواد گوشتی فراوری شده افزوده می شود و بالاخره اینکه نیترات در ارگانیسم نیز کم و بیش قابل تبدیل شدن به نیتریت است، ولی با توجه به امکان تبدیل نیترات به نیتریت در بدن است که نیتراتِ- به خودی خود “بی خطر یا حداکثر کم خطر”- درگروه مواد خطر ناک برای سلامتی طبقه بندی می شود.
نیتریت درغذای نوزادان و خطرات آن
ابتدا کمی به گذشته ها بر می گردیم :
“در سال 2003 در اطلاعیه آزمایشگاه استانی بازل (Basel) سوئیس نسبت به استفاده از سبزیجات با نیترات بالا در غذای کودکان هشدار داده شد! در آن تاریخ در بازِل سوئیس یک نوزاد 8 ماهه در بیمارستان بستری شد. پزشکان بیماری این نوزاد را”کبودی”یا سیانوز (cyanosis )، یک بیماری خطرناک تشخیص دادند که با کمبود اکسیژن در خون مرتبط است” آزمایشگاه مذکور در گزارش خود به این موضوع اشاره می کند که ” علت ابتلاء این نوزاد به این بیماری یک غذای کودک است که با استفاده از مقدار زیادی کلم قمری (Kohlrabi) در خانه آماده شده است”
در همان سال ها و پس از این تشخیص توصیه شد که درتهیه غذای نوزاد از محصولاتی با در صد بالا از نتیرات استفاده نشود، زیرا خطر یک مسمومیت حاد وجود خواهد داشت. در ادامه تأکید شد که در غذای نوزاد از اسفناج و کاهو استفاده نشود.
منبع : https://www.seilnacht.com/Lexikon/Nitrate.htm
Thomas Seilnacht, veröffentlicht in chimica didactica 1995, Heft 3
مکانیسم ایجاد بیماری سیانوز در نوزادان
هموگلوبین، ماده عامل انتقال اکسیژن در خون، می تواند در نوزادان تا سه ماهگی به وسیله نیتریت دچار تغییر در ساختار شده و به « مِت هموگلوبین» (methemoglobin) تبدیل شود. مِت هموگلوبین درساختار، بجای اکسیژن آب به عنوان لیگاند دارد و اگر چه قادر به جذب اکسیژن است، ولی قادر به انتقال و پس دادن آن به بافت ها نبوده و سلول ها و بافت های مصرف کننده اکسیژن را با فقدان آن مواجه می کند. این نارسائی عامل به وجود آمدن مشکلاتی از جمله اختلال در تنفس( خفگی) یا بیماری سیانوز(cyanosis) است که خود را با آبی رنگ شدن( اصطلاحاً کبود شدن) پوست، بخصوص لب ها نشان می دهد دراینجا لازم است اشاره شود که اگرچه تبدیل مِت هموگلوبین به هموگلوبین از طریق یک آنزیم مخصوص بنام methemoglobin reductase امکان پذیر است، ولی میزان این آنزیم در نوزادان تا حدود 6 ماهگی( هنوز) بقدر کافی وجود ندارد.
منبع : « سازمان ایمنی غذایی اروپا » (EFSA) ؛ سال 2008
از نکات مهم مرتبط با بیماری کبودی در نوزادان در آن سال ها این بود که در آن دوران دربرخی از مناطق روستائی میزان نیترات در آب بین 200 تا بعضاً 500 میلی گرم بر لیتربود و چون از همین آب در تهیه غذای نوزان نیزاستفاده می گردید ، بیماری سیانوز نیز وجود داشت. در سال های بعد که میزان نیترات در آب کنترل و کاهشی شد، بیماری سیانوز (در نوزادان) نیز به طور قابل ملاحظه ای کاهش یافت.
از بیماری سیانوز در نوزادن که بگذریم ، لازم است تأکید گردد که خطرآفرینی عمده نیتریت- در گذشته و حال- زمانی ست که این ترکیب با آمین های نوع دوم (secondary amines) در معده، نیتروزوآمین-ترکیبی سرطان زا- ایجاد می کند.
( در بخش نیتروزو آمین توضیح داده شده است)
نیتروزوآمین ها
نیتروزوآمین ها یا دقیق تر، اِن نیتروزو آمین ها (N‑Nitrosamines ) مشتقاتی از آمین های نوع دوم (secondary amines) می باشند که به وسیله ترکیبات نیتروزو کننده مانند ” نیترو اسید ” (نیتروس اسید) و املاح آن، ایجاد می شوند .
این ترکیبات نیتروزو آمینی به علت سرطان زایی بالایی که دارند، بسیار مورد توجه- درحد نفرت !- قرار گرفته اند.
ساده ترین نوع از انواع این گروه از ترکیبات ، ترکیب اِن نیتروزو دی متیل آمین (NNDMA) است .
نحوه ایجاد یک نیتروزو آمین ساده در بدن
نیترات ها در بزاق دهان افراد بالغ معمولاً در مقادیر اندک به نیتریت تبدیل می شوند. نیتریت سپس می تواند در صورت وجود ترکیبات آمینی- معمولاً آمین های نوع دوم (secondary amines )- به نیتروزو آمین تبدیل گردد. در هرصورت و بدون در نظر گرفتن منبع نیتریت نیز همچنین قادرند نیتروزو آمین ها در محیط ( معمولاً ) اسیدی معده از مسیر تبدیل اولیه نیترات به نیتریت و سپس” نیترو اسید ” (نیتروس اسید)(HNO2) تبدیل گردد. این ترکیب سپس و مجدداً در محیط اسیدی یک پروتون جذب کرده و به نیتروزیلکاتیون تبدیل میگردد. اکنون این نیتروزیل کاتیون با ترکیب با یک آمین نوع دوم به نیتروزو آمین تبدیل می شود. (تصویر)

نیتروزو آمین ها همچنین در آتمسفر به واسطه وجود برخی از آمین های” مناسب” و اکسید های نیتروژن از طریق واکنش های فتو شیمیایی ایجاد می شوند.
نیتروزو آمین ها و خطرات آنها
این ترکیبات می توانند در مقادیر (حتی) اندک، عاملی برای بیماری سرطان باشند. سازمان بهداشت جهانی (WHO ) اعلام می دارد که روزانه (می تواند) حداکثر 220 میلی گرم نیترات از (مسیرهای مختلف) وارد بدن شود. براساس استانداردهای مرتبط با آب آشامیدنی درآلمان، حداکثر وجود 50 میلی گرم بر لیترمجاز است. برای اتریش وضعیت مشابه آلمان است و در سوئیس این میزان 40 میلی گرم تعیین شده است. این ارقام ولی می توانند برای نوزادان خطر آفرین باشند و از این رو توصیه بر استفاده از آب معدنی” کم نیترات” در تهیه غذا برای نوزادان گردیده است .
جزئیات بیشتر در باره مکانیسم سرطان زائی

در 90% آزمایشات انجام شده روی حیوانات آزمایشگاهی، ترکیبات نیتروزو آمینی به وضوح سرطان زا تشخیص داده شدند. نیتروزو آمین ها در کاتگوری ترکیبات « پیش سرطان زا » ( precancerogens )قرار دارند، بدین معنی که می بایست برای ” دست بکار شدن”، در بدن ابتدا فعال شوند تا قادر به ” اثر گذاری بی برو برگرد” باشند! این مکانیسم از طریق واکنش های کاتالیست شده به وسیله آنزیمی با عنوان ” cytochrom-P450 ” رخ می دهد، بدین ترتیب که در ابتدای کار ماده بسیار واکنش گرای فرم آلدهید و مهمتر از آن، ترکیباتی موسوم به “کاربونیوم یون ها” (carbonium ions) آزاد می شوند.
تحقیقات دامنه داری که روی چگونگی سرطان زایی نیتروزو دی آلکیل آمین انجام شده است، حاکی از آن است که در بدن ابتدا متابولیتی با نام « آلکیل دی آزو هیدروکسیل» ایجاد می شود که ماده ” اصلی ” برای ایجاد سرطان است، بدین ترتیب که با آزاد سازی نیتروژن، کاربو نیو م یون (ها) (carbonium ions) به وجود می آیند. این ترکیباتِ بسیار واکنش گرایِ حاوی یون« متیل کاتیون » سپس به دی اِن ای (DNA) و آر اِن اِی (RNA) متصل شده و آداکت هائی را تشکیل می دهند. جزئیات بیشتر حاکی از آن است که ( به عنوان مثال) اِن نیتروزو دی متیل آمین (N-Nitrosodimethylamin) به وضوح بازهای دی اِن ای- گوآنین و آدنین- را متیله کرده و باعث ایجاد تغییرات گسترده در دی اِن اِی (DNA ) می شوند. این تغییرات به عنوان عامل اصلی بروز سرطان ارزیابی گردیده اند. ( پرداختن به جزئیات بیشتراین مقوله درحوصله این مقاله نمی گنجد)
محصولات گوشتی فراوری شده و نیتروزو آمین ها

احتیاط در تناول غذاهای گوشتی “گریل” شده از” اوجب واجبات” است !
یکی دیگر از” منابع ” تولید نیتروزو آمین ها، گوشت و مواد گوشتی، به ویژه انواع فراوری شده آن از جمله سوسیس و کالباس است. در این محصولات (بطور معمول) از نگهدارنده های حاوی نیترات و/ یا نیتریت موسوم به ” افزودنی های مجاز” ( در اتحادیه اروپا ؛ در ایران را نمی دانم ! ) استفاده می شود.
شماره های افزودنی های مجاز : E 250 (سدیم نیتریت )؛ E 251 ( سدیم نیترات ) و E 252 ( پتاسیم نیترات )
با داغ کردن این محصولات گوشتی- بخصوص در روش “گریل” (و دود حاصل از آن)- نیترات و/ یا نیتریت موجود، با آمین های درون گوشت واکنش کرده و”جناب نیتروزوآمین”سرو کله اش پیدا می شود. مکانیسم این پروسه در بالا تشریح گردید. کل این ” ماجرا ” زمانی ” اثرگذارتر” می شود که به سوسیس و کالباس برای خوشمزه ترشدن ، پنیر – بخصوص از نوع حاوی آمین نیز اضافه می شود.
یک نکته مهم در خصوص استفاده از مواد نگهدارنده فوق الذکر(E 249 – E 252) دربرخی از محصولات غذائی مانند پنیرهای ” سخت” که در پخت و پز انواع پیتزا، ماکارونی، اسپاگتی، ژامبون و… استفاده می شود، لازم است اشاره شود که در زمان “تنوری شدن” یا حتی حرارت دادن ساده این محصولات نیز نیتروزو آمین ایجاد می شود .
منابع و ارجاعات را در وبلاگ علوم و تکنولوژی رنگ دنبال کنید.






